Bayangkan skenario ini: seseorang masuk rumah sakit dengan infeksi bakteri yang seharusnya mudah ditangani. Dokter meresepkan antibiotik standar. Namun setelah beberapa hari, kondisi pasien tidak membaik — bakteri penyebab infeksi ternyata tidak mempan dengan antibiotik yang tersedia. Skenario ini bukan fiksi ilmiah. Ia terjadi setiap hari, di hampir setiap negara di dunia, termasuk Indonesia.
Inilah wajah nyata dari resistensi antimikroba (antimicrobial resistance, AMR) — salah satu ancaman kesehatan paling serius abad ke-21 yang sering kali tak terlihat namun dampaknya terasa sangat nyata.
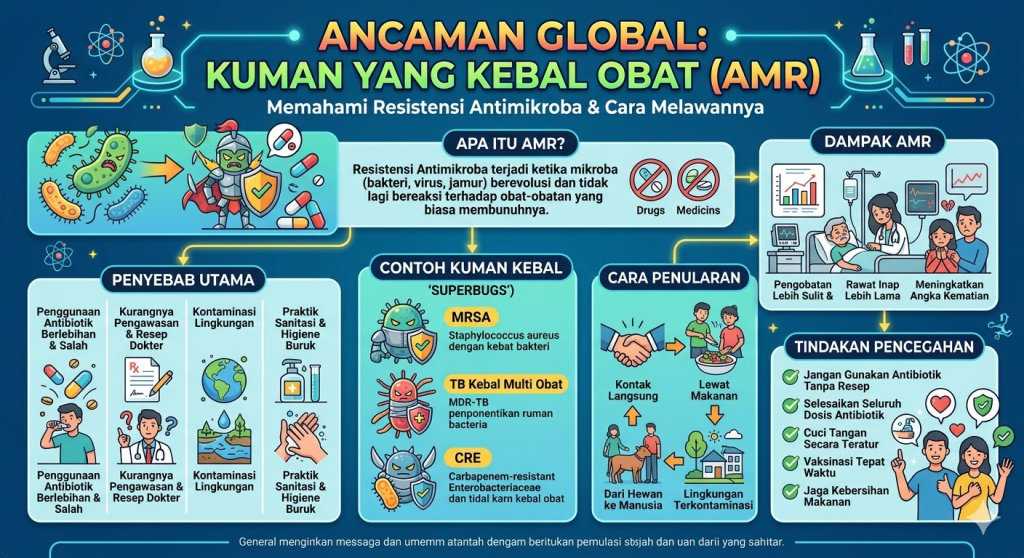
Apa Itu Resistensi Antimikroba?
Antimikroba adalah kelompok obat yang digunakan untuk melawan infeksi yang disebabkan oleh mikroorganisme — meliputi bakteri, virus, jamur, dan parasit. Antibiotik adalah golongan yang paling dikenal, khusus digunakan melawan infeksi bakteri. Sedangkan antivirus, antijamur, dan antiparasit masing-masing digunakan untuk menangani infeksi oleh kelompok mikrobanya.
Resistensi antimikroba terjadi ketika mikroorganisme berkembang sedemikian rupa sehingga obat yang sebelumnya efektif tidak lagi mampu membunuh atau menghambat pertumbuhannya. Ini bukan tubuh manusia yang menjadi kebal terhadap obat, melainkan mikrobanya sendiri yang berevolusi dan mengembangkan mekanisme pertahanan baru. Ketika seorang pasien dikatakan “kebal antibiotik,” yang dimaksud sebenarnya adalah bakteri penyebab infeksinya yang sudah tidak dapat diatasi oleh antibiotik tersebut.
Mekanisme resistensi ini beragam. Bakteri bisa memproduksi enzim yang merusak antibiotik sebelum obat sempat bekerja, mengubah struktur reseptornya sehingga antibiotik tidak lagi dapat menempel, atau memompa keluar antibiotik yang sudah masuk ke dalam selnya (efflux pump). Pada jamur, resistensi juga terjadi melalui mutasi genetik, duplikasi gen, hingga perubahan komposisi dinding dan membran sel (Kadariswantiningsih et al., 2025).
Yang memperparah situasi, gen resistensi ini dapat berpindah antarbakteri melalui proses yang disebut horizontal gene transfer — artinya resistensi bisa menyebar antar spesies bakteri yang berbeda, bahkan dari bakteri yang tidak berbahaya ke bakteri yang berbahaya.
Seberapa Besar Ancamannya?
Data terbaru memberikan gambaran yang mengkhawatirkan. Sebuah analisis sistematis komprehensif yang diterbitkan di The Lancet pada tahun 2024 — mencakup data dari 204 negara dan 520 juta rekam medis individu dari tahun 1990 hingga 2021 — menemukan bahwa pada tahun 2021, sebanyak 4,71 juta kematian di seluruh dunia berkaitan dengan infeksi bakteri yang resisten terhadap obat. Dari angka tersebut, 1,14 juta kematian secara langsung disebabkan oleh resistensi antimikroba itu sendiri — bukan oleh infeksinya semata, melainkan karena bakterinya tidak bisa diatasi dengan obat yang tersedia (IHME Global Burden of Disease Collaborators, 2024).
Proyeksi ke depan pun tidak menggembirakan. Pada tahun 2050, diperkirakan jumlah kematian yang langsung disebabkan AMR akan mencapai 1,91 juta per tahun, sementara kematian yang berkaitan dengan AMR bisa mencapai 8,22 juta jiwa per tahun. Kawasan Asia Selatan dan Amerika Latin diproyeksikan akan menanggung beban terbesar. Kelompok usia yang paling terdampak bukan lagi anak-anak, melainkan lansia berusia 70 tahun ke atas — sejalan dengan tren penuaan populasi global (IHME Global Burden of Disease Collaborators, 2024).
Ada satu kabar yang sedikit menggembirakan: kematian akibat AMR pada anak di bawah usia lima tahun justru menurun lebih dari 50% dalam rentang 1990–2021. Hal ini menunjukkan bahwa perbaikan akses layanan kesehatan anak, vaksinasi, dan higiene memang memberikan hasil nyata. Namun di sisi lain, kematian AMR pada kelompok dewasa dan lansia justru meningkat pesat.
Mikroba Apa Saja yang Paling Perlu Diwaspadai?
Organisasi Kesehatan Dunia (WHO) secara berkala menerbitkan daftar prioritas patogen bakteri resisten yang paling mengancam — WHO Bacterial Priority Pathogens List (BPPL). Daftar terbaru yang dirilis pada tahun 2024, dipublikasikan dalam The Lancet Infectious Diseases, menggunakan pendekatan analisis multikriteria yang melibatkan 78 pakar internasional dari berbagai latar belakang dan wilayah geografi (Sati et al., 2025).
Berdasarkan daftar prioritas WHO 2024, bakteri yang masuk kategori critical (prioritas tertinggi) antara lain:
- Klebsiella pneumoniae yang resisten terhadap karbapenem (menduduki peringkat pertama dengan skor 84%)
- Acinetobacter spp. yang resisten terhadap karbapenem
- Escherichia coli yang resisten terhadap karbapenem dan sefalosporin generasi ketiga
- Mycobacterium tuberculosis yang resisten terhadap rifampisin (TB-MDR/XDR)
Kategori high priority mencakup, di antaranya, Pseudomonas aeruginosa resisten karbapenem dan Staphylococcus aureus yang resisten terhadap metisilin — dikenal dengan singkatan MRSA (Methicillin-Resistant Staphylococcus aureus).
Daftar ini juga menyoroti bakteri yang umum menyebabkan infeksi di komunitas, seperti Salmonella Typhi yang resisten fluorokuinolon (penyebab tifus), Shigella spp., dan Neisseria gonorrhoeae resisten fluorokuinolon (penyebab gonore) — ketiganya masuk dalam kategori high priority. Fakta ini relevan untuk Indonesia, mengingat tifus dan gonore masih menjadi masalah kesehatan yang signifikan di negara kita.
Resistensi terhadap karbapenem — golongan antibiotik yang selama ini dianggap sebagai “senjata terakhir” untuk infeksi berat — meningkat sangat mengkhawatirkan. Kematian yang berkaitan dengan resistensi karbapenem pada bakteri Gram-negatif meningkat dari 619.000 jiwa pada 1990 menjadi lebih dari 1 juta jiwa pada 2021 (IHME Global Burden of Disease Collaborators, 2024).
Tidak hanya bakteri — ancaman resistensi antijamur juga semakin nyata. Peneliti dari Universitas Airlangga menyoroti bahwa resistensi antijamur berkembang melalui mekanisme intrinsik (seperti aktivitas pompa efflux yang tinggi dan komposisi unik dinding sel jamur) maupun mekanisme yang diperoleh melalui mutasi genetik. Kemampuan sel jamur untuk bertahan hidup pada konsentrasi obat yang tinggi mempersulit penanganan klinis (Kadariswantiningsih et al., 2025).
Bagaimana Resistensi Bisa Berkembang?
Resistensi antimikroba adalah produk dari evolusi — proses alami yang dipercepat secara dramatis oleh perilaku manusia. Ketika antibiotik digunakan, ia tidak hanya membunuh bakteri yang menjadi target, tetapi juga membunuh bakteri komensal (bakteri “baik” yang hidup di tubuh kita secara normal). Yang tersisa adalah bakteri-bakteri yang secara kebetulan memiliki gen resistensi — mereka kemudian berkembang biak tanpa persaingan dari bakteri lain. Inilah yang disebut selective pressure atau tekanan seleksi.
Beberapa perilaku yang mempercepat proses ini antara lain:
Penggunaan antibiotik yang tidak tepat. Meminum antibiotik untuk infeksi virus (seperti flu biasa, batuk pilek, dan sebagian besar radang tenggorokan) tidak memberikan manfaat apapun bagi pasien, namun secara aktif menciptakan tekanan seleksi pada bakteri di tubuh pasien. Peraturan Menteri Kesehatan RI Nomor 28 Tahun 2021 tentang Pedoman Penggunaan Antibiotik secara tegas menekankan bahwa antibiotik yang tidak digunakan secara bijak dapat memicu timbulnya masalah resistensi, dan penggunaan bijak berarti mempertimbangkan dampak muncul serta menyebarnya bakteri resisten.
Tidak menyelesaikan pengobatan antibiotik sesuai dosis. Ketika seseorang berhenti minum antibiotik begitu gejala membaik — padahal kursus pengobatan belum selesai — bakteri yang paling tahan terhadap antibiotik bisa saja bertahan hidup, berkembang biak, dan menjadi populasi yang resisten.
Pembelian antibiotik tanpa resep. Di banyak negara berkembang, termasuk Indonesia, antibiotik masih bisa dibeli bebas di apotek tanpa resep dokter. Data menunjukkan nilai penjualan antibiotik di Indonesia mencapai Rp 10,4 triliun pada 2022, menjadikannya golongan obat resep dengan nilai penjualan terbesar — sebuah angka yang mencerminkan betapa masifnya penggunaan antibiotik di luar kendali resep dokter.
Penggunaan berlebihan dalam peternakan dan pertanian. Inilah dimensi yang sering kali luput dari perhatian publik, namun krusial.
One Health: Masalah Manusia, Hewan, dan Lingkungan
AMR bukan hanya masalah dunia kedokteran manusia. Ia adalah masalah lintas batas yang melibatkan kesehatan manusia, kesehatan hewan, dan kesehatan lingkungan secara bersamaan. Konsep ini dikenal sebagai One Health — satu kesehatan.
Sebuah tinjauan yang diterbitkan dalam Science in One Health (2024) menegaskan bahwa pengurangan penggunaan antimikroba di sektor pertanian dan peternakan adalah salah satu strategi kunci dalam mengendalikan AMR secara global. Upaya lain yang disorot meliputi peningkatan akses terhadap air bersih dan sanitasi (WASH), penguatan Universal Health Coverage (UHC), dan pengendalian infeksi yang lebih ketat di fasilitas layanan kesehatan (Woolhouse, 2024).
Di sektor peternakan, antibiotik sering digunakan bukan hanya untuk mengobati hewan yang sakit, tetapi juga sebagai growth promoter — pemacu pertumbuhan — dan sebagai profilaksis massal. Praktik ini menciptakan kolam gen resistensi yang sangat besar di lingkungan. Surveilans bakteri resisten multi-obat yang dilakukan oleh Perhimpunan Dokter Spesialis Patologi Klinik dan Kedokteran Laboratorium Indonesia di 41 rumah sakit di Indonesia pada 2018 telah mengidentifikasi keberadaan MRSA, bakteri penghasil ESBL (Extended Spectrum Beta-Lactamases), VRE (Vancomycin-Resistant Enterococcus), dan bakteri yang resisten terhadap karbapenem.
Gen resistensi dari bakteri hewan ternak dapat berpindah ke manusia melalui berbagai jalur: konsumsi produk pangan asal hewan, kontak langsung dengan hewan atau lingkungannya, hingga kontaminasi air dan tanah oleh kotoran hewan yang mengandung bakteri resisten. Sebuah editorial dalam Frontiers in Microbiology (2023) menekankan bahwa pendekatan One Health — yang mengintegrasikan respons dari sektor pertanian, lingkungan, dan kesehatan manusia — adalah satu-satunya cara yang realistis untuk mengatasi AMR secara komprehensif (Li et al., 2023).
Bakteri seperti Enterococcus spp., yang umum ditemukan pada manusia, hewan ternak, dan lingkungan, menjadi indikator penting penyebaran resistensi lintas sektor ini. Bakteri ini menunjukkan bagaimana gen resistensi dapat bermigrasi melalui rantai makanan dan ekosistem (Zaidi et al., 2024).
Situasi di Indonesia: Tantangan yang Belum Terselesaikan
Indonesia menghadapi tantangan berlapis dalam mengatasi AMR. Pertama, beban penyakit infeksi yang masih tinggi mendorong penggunaan antibiotik yang masif. Kedua, regulasi yang ada belum diimplementasikan secara optimal.
Dari sisi regulasi, Indonesia sebenarnya telah memiliki kerangka hukum yang cukup baik. Peraturan Menteri Kesehatan Nomor 28 Tahun 2021 tentang Pedoman Penggunaan Antibiotik diterbitkan untuk mewujudkan pengendalian resistensi antimikroba, penggunaan antibiotik yang tepat, efektif, efisien, dan aman dalam pelayanan kesehatan, serta penggunaan obat secara rasional di Indonesia. Regulasi ini memperbarui pedoman sebelumnya (Permenkes No. 2406/2011) dan mengintegrasikan sistem klasifikasi AWaRe dari WHO.
Klasifikasi AWaRe membagi antibiotik ke dalam tiga kelompok:
- ACCESS: Antibiotik lini pertama yang tersedia di semua fasilitas kesehatan, untuk infeksi bakteri umum
- WATCH: Antibiotik lini kedua yang hanya boleh digunakan untuk indikasi tertentu di fasilitas yang lebih lengkap
- RESERVE: Antibiotik “senjata terakhir” yang hanya boleh digunakan pada infeksi yang telah terbukti resisten terhadap semua pilihan lain, dengan pengawasan ketat
Klasifikasi ini bertujuan memperpanjang usia efektivitas antibiotik dengan memastikan bahwa antibiotik yang lebih kuat tidak digunakan sembarangan.
Di tingkat rumah sakit, Permenkes No. 8 Tahun 2015 mengamanatkan setiap rumah sakit untuk membentuk Tim PPRA — Tim Program Pengendalian Resistensi Antimikroba. Tim ini bertugas mengawasi penggunaan antibiotik, menyusun panduan penggunaan antibiotik (PPAB), dan memantau pola resistensi di fasilitas masing-masing. Namun kenyataannya, Kementerian Kesehatan hanya menerima laporan dari 152 rumah sakit dari sekitar 3.000 rumah sakit yang seharusnya menjalankan PPRA selama periode 2020–2023.
Kesenjangan antara regulasi dan implementasi ini menjadi tantangan utama. Dari sisi rantai pangan, penggunaan antibiotik di sektor peternakan dan akuakultur di Indonesia juga masih perlu pengawasan yang lebih ketat dalam konteks pendekatan One Health.
Langkah Nyata: Apa yang Bisa Dilakukan?
Di Tingkat Kebijakan dan Fasilitas Kesehatan
Bukti dari berbagai negara menunjukkan bahwa program penatagunaan antibiotik (antimicrobial stewardship program) yang diimplementasikan dengan baik memberikan hasil nyata. Sebuah studi di rumah sakit komunitas di Italia mendapati bahwa pelaksanaan program stewardship selama setahun berhasil mengurangi angka kematian akibat infeksi sebesar 8,8%, menurunkan angka rawat ulang dalam sebulan sebesar 19%, dan memangkas biaya antibiotik rata-rata hingga 35% per pasien (Albano et al., 2023).
Kunci keberhasilan program ini mencakup pengawasan penggunaan antibiotik “kritis,” pengembangan panduan penggunaan antibiotik berbasis bukti, pelatihan berkelanjutan bagi tenaga kesehatan, dan audit kualitas penggunaan antibiotik secara rutin.
Di Indonesia, penguatan implementasi PPRA di seluruh rumah sakit — bukan hanya 152 yang melaporkan, tetapi semua — adalah langkah mendesak. Ini memerlukan komitmen kuat dari manajemen rumah sakit dan dukungan penuh dari Kementerian Kesehatan, termasuk umpan balik yang bermakna terhadap laporan yang sudah diberikan.
Penguatan surveilans AMR nasional juga sangat diperlukan. Data resistensi yang akurat dan mutakhir dari berbagai wilayah di Indonesia akan memungkinkan penyesuaian panduan pengobatan yang lebih relevan dengan kondisi lokal.
Di Tingkat Masyarakat dan Pasien
Peran individu tidak bisa diremehkan. Berikut beberapa hal yang dapat dilakukan setiap orang:
Jangan meminta atau menggunakan antibiotik untuk infeksi virus. Flu, pilek, sebagian besar batuk, dan radang tenggorokan tanpa komplikasi umumnya disebabkan oleh virus — antibiotik tidak akan membantu, bahkan bisa merugikan dengan mendorong resistensi. Dokter yang tidak meresepkan antibiotik untuk kondisi-kondisi ini bukan berarti tidak peduli; justru sebaliknya.
Tuntaskan pengobatan antibiotik sesuai anjuran dokter. Jika dokter meresepkan antibiotik selama tujuh hari, minumlah selama tujuh hari penuh — meskipun Anda sudah merasa lebih baik di hari ketiga atau keempat. Menghentikan pengobatan lebih awal bisa meninggalkan bakteri yang masih hidup namun sudah terpapar antibiotik, memberi mereka “kesempatan belajar” untuk menjadi resisten.
Jangan berbagi atau menyimpan antibiotik sisa. Antibiotik yang tersisa dari pengobatan sebelumnya tidak boleh digunakan sendiri untuk kondisi yang tampaknya serupa, apalagi diberikan kepada orang lain. Diagnosis yang tepat oleh dokter tetap diperlukan.
Jaga higiene dan sanitasi. Cuci tangan secara rutin, konsumsi makanan yang dimasak dengan benar, dan pastikan sumber air yang digunakan bersih. Mencegah infeksi berarti mengurangi kebutuhan akan antibiotik.
Lengkapi vaksinasi. Vaksin mencegah infeksi sehingga mengurangi kebutuhan antibiotik. Vaksin pneumokokus, misalnya, melindungi dari salah satu bakteri penyebab pneumonia yang serius; vaksin Hib melindungi dari Haemophilus influenzae tipe B. Semakin sedikit infeksi yang terjadi, semakin sedikit antibiotik yang digunakan, semakin lambat perkembangan resistensi.
Masa Depan: Harapan di Antara Tantangan
Apakah ada harapan? Ya — meskipun jalan ke depan tidak mudah.
Di garis penelitian, beberapa kelas antibiotik baru sedang dalam tahap pengembangan. Sejak daftar prioritas patogen WHO pertama kali diterbitkan pada 2017, setidaknya 13 antibiotik baru yang menyasar bakteri dalam daftar tersebut telah mendapatkan persetujuan edar (Sati et al., 2025). Meski ini kabar baik, laju penemuan antibiotik baru masih jauh lebih lambat dibandingkan laju berkembangnya resistensi.
Pendekatan non-antibiotik juga menjanjikan: fag terapi (bacteriophage therapy) yang menggunakan virus pemakan bakteri, pengembangan vaksin melawan bakteri yang kini resisten, probiotik untuk memulihkan ekosistem mikroba normal, serta diagnostik cepat yang memungkinkan dokter menentukan jenis dan sensitivitas bakteri sebelum memilih antibiotik.
Analisis dari studi GBD 2024 memperkirakan bahwa jika akses terhadap perawatan infeksi yang baik meningkat secara global — termasuk akses terhadap antibiotik yang tepat, bukan antibiotik sembarangan — sebanyak 92 juta kematian bisa dicegah secara kumulatif antara tahun 2025 hingga 2050. Ini bukan angka yang kecil. Ini adalah jutaan nyawa yang bergantung pada keputusan kolektif yang kita buat hari ini: kebijakan yang kita terapkan, obat yang kita minum dengan bijak, dan makanan yang kita produksi dengan bertanggung jawab (IHME Global Burden of Disease Collaborators, 2024).
AMR adalah masalah bersama — bukan hanya urusan dokter atau pemerintah. Setiap pilihan yang kita buat soal antibiotik, baik sebagai pasien, sebagai tenaga kesehatan, sebagai peternak, maupun sebagai konsumen produk pangan, turut membentuk lanskap resistensi yang akan dihadapi generasi mendatang.
Daftar Referensi
Albano, G. D., Midiri, M., Zerbo, S., Matteini, E., Passavanti, G., Curcio, R., Curreri, L., Albano, S., Argo, A., & Cadelo, M. (2023). Implementation of a year-long antimicrobial stewardship program in a 227-bed community hospital in Southern Italy. International Journal of Environmental Research and Public Health, 20(2), 996. https://doi.org/10.3390/ijerph20020996
IHME Global Burden of Disease Collaborators. (2024). Global burden of bacterial antimicrobial resistance 1990–2021: A systematic analysis with forecasts to 2050. The Lancet, 404(10459), 1199–1226. https://doi.org/10.1016/S0140-6736(24)01867-1
Kadariswantiningsih, I. N., Empitu, M. A., Santosa, T. I., & Alimu, Y. (2025). Antifungal resistance: Emerging mechanisms and implications (Review). Molecular Medicine Reports, 32(3). https://doi.org/10.3892/mmr.2025.13612
Kementerian Kesehatan Republik Indonesia. (2015). Peraturan Menteri Kesehatan Nomor 8 Tahun 2015 tentang Program Pengendalian Resistensi Antimikroba di Rumah Sakit. Kemenkes RI.
Kementerian Kesehatan Republik Indonesia. (2021). Peraturan Menteri Kesehatan Nomor 28 Tahun 2021 tentang Pedoman Penggunaan Antibiotik. Kemenkes RI.
Li, T., Hao, H., Hou, X., & Xia, J. (2023). Editorial: Antimicrobial resistance: Agriculture, environment and public health within One Health framework. Frontiers in Microbiology, 14, 1252134. https://doi.org/10.3389/fmicb.2023.1252134
Sati, H., Carrara, E., Savoldi, A., Hansen, P., Garlasco, J., Campagnaro, E., … Tacconelli, E. (2025). The WHO Bacterial Priority Pathogens List 2024: A prioritisation study to guide research, development, and public health strategies against antimicrobial resistance. The Lancet Infectious Diseases, 25(9), 1033–1043. https://doi.org/10.1016/S1473-3099(25)00118-5
Woolhouse, M. E. J. (2024). One Health approaches to tackling antimicrobial resistance. Science in One Health, 3, 100082. https://doi.org/10.1016/j.soh.2024.100082
Zaidi, S., Zaheer, R., Zovoilis, A., & McAllister, T. A. (2024). Enterococci as a One Health indicator of antimicrobial resistance. Canadian Journal of Microbiology, 70(8), 303–335. https://doi.org/10.1139/cjm-2024-0024

Tinggalkan komentar