Polip usus adalah pertumbuhan jaringan abnormal yang muncul dari lapisan mukosa dinding usus besar (kolon) atau rektum, menonjol ke arah lumen usus. Sebagian besar polip bersifat jinak dan tidak menimbulkan gejala. Namun, di balik penampilannya yang tampak tidak berbahaya, beberapa jenis polip memiliki potensi untuk berubah menjadi kanker kolorektal — salah satu kanker paling mematikan di dunia. Pemahaman yang baik tentang polip usus, mulai dari jenis, faktor risiko, hingga tata laksananya, menjadi kunci penting dalam upaya pencegahan kanker kolorektal.
Seberapa Sering Polip Usus Ditemukan?
Polip kolorektal merupakan temuan yang sangat umum dalam pemeriksaan kolonoskopi. Data epidemiologis menunjukkan bahwa prevalensi adenoma pada populasi usia skrining (umumnya di atas 50 tahun) berkisar antara 20% hingga 60% pada studi kolonoskopi, dan prevalensi ini meningkat seiring bertambahnya usia (Sullivan et al., 2022). Pada pasien tanpa gejala dengan risiko rata-rata, prevalensi adenoma rata-rata sekitar 10% pada studi sigmoidoskopi dan lebih dari 25% pada studi kolonoskopi (Correa, 2005).
Di Indonesia, data skrining kanker kolorektal berbasis layanan kesehatan primer di Semarang, Jawa Tengah, menunjukkan bahwa dari pasien yang menjalani kolonoskopi setelah tes darah samar tinja positif, tingkat deteksi polip mencapai 30,8% dan tingkat deteksi adenoma (adenoma detection rate/ADR) sebesar 26,9% (Purnomo et al., 2023). Angka insiden kanker kolorektal di Indonesia yang terstandarisasi usia dilaporkan sebesar 15,9 per 100.000 untuk laki-laki dan 10,1 per 100.000 untuk perempuan (Sinaga et al., 2021). Meskipun Indonesia tergolong negara dengan prevalensi kanker kolorektal yang relatif lebih rendah dibandingkan negara-negara Asia seperti Jepang dan Korea, tren peningkatan insiden — terutama pada populasi usia muda — menjadi perhatian serius (Makmun et al., 2021).
Memahami Jenis-Jenis Polip Usus
Tidak semua polip diciptakan sama. Klasifikasi polip usus berdasarkan histopatologinya sangat menentukan potensi keganasan dan pendekatan tata laksananya. Secara garis besar, polip kolorektal dapat dikelompokkan menjadi dua jalur utama: jalur adenoma konvensional dan jalur polip serasi (serrated polyp pathway).
Polip adenomatosa merupakan jenis polip neoplastik yang paling umum dan merupakan prekursor utama kanker kolorektal melalui jalur yang dikenal sebagai rangkaian adenoma-karsinoma (adenoma-carcinoma sequence). Berdasarkan gambaran histologisnya, adenoma dibagi menjadi tubular (paling umum dan risiko terendah), tubulovilosa, dan vilosa (risiko tertinggi untuk keganasan). Adenoma dengan ukuran ≥10 mm, mengandung komponen vilosa, atau menunjukkan displasia tingkat tinggi (high-grade dysplasia) dikategorikan sebagai adenoma lanjut (advanced adenoma), yang memiliki risiko lebih tinggi untuk berkembang menjadi kanker (Sullivan et al., 2022; Gupta et al., 2020).
Polip serasi dahulu dianggap hanya sebagai polip hiperplastik yang tidak berpotensi ganas. Namun, pemahaman ini telah berubah drastis dalam dua dekade terakhir. Jalur neoplasia serasi (serrated neoplastic pathway) kini diakui sebagai jalur penting menuju kanker kolorektal, terutama terkait dengan kanker interval yang muncul di antara jadwal skrining. Polip serasi dibagi menjadi tiga subtipe utama: polip hiperplastik (hyperplastic polyp/HP) yang umumnya jinak dan berukuran kecil di rektum atau kolon sigmoid, lesi serasi sesil (sessile serrated lesion/SSL) yang memiliki potensi keganasan bermakna terutama jika berukuran ≥10 mm atau mengandung displasia, serta adenoma serasi tradisional (traditional serrated adenoma/TSA) yang lebih jarang ditemukan (Crockett & Nagtegaal, 2019; Murakami et al., 2022).
Selain kedua kelompok tersebut, terdapat polip non-neoplastik lain seperti polip inflamatorik yang umum ditemukan pada penyakit radang usus (inflammatory bowel disease) dan polip hamartomatosa yang terkait dengan sindrom poliposis herediter seperti sindrom Peutz-Jeghers dan poliposis juvenil.
Bagaimana Polip Terbentuk?
Pembentukan polip usus melibatkan akumulasi mutasi genetik yang menyebabkan pertumbuhan sel-sel mukosa usus menjadi tidak terkendali. Pada jalur adenoma konvensional, mutasi awal biasanya terjadi pada gen adenomatous polyposis coli (APC), yang merupakan gen penekan tumor. Mutasi ini diikuti oleh mutasi sekuensial pada gen-gen lain seperti KRAS, SMAD4, dan TP53, yang secara bertahap mendorong progresi dari mukosa normal menjadi adenoma dan akhirnya karsinoma.
Pada jalur serasi, mekanisme molekulernya berbeda. Mutasi pada onkogen BRAF dan metilasi promoter DNA (CpG island methylator phenotype/CIMP) memainkan peran sentral. Lesi serasi sesil cenderung berkembang menjadi kanker kolorektal dengan instabilitas mikrosatelit (microsatellite instability/MSI) tinggi, yang memiliki karakteristik biologis dan prognostik yang berbeda dari kanker yang berkembang melalui jalur adenoma konvensional (Crockett & Nagtegaal, 2019).
Siapa yang Berisiko?
Faktor risiko polip usus bersifat multifaktorial, melibatkan kombinasi faktor yang tidak dapat dimodifikasi dan faktor yang dapat dimodifikasi.
Faktor yang tidak dapat dimodifikasi meliputi usia (risiko meningkat signifikan setelah usia 50 tahun), jenis kelamin laki-laki, riwayat keluarga dengan kanker kolorektal atau polip adenomatosa, serta predisposisi genetik termasuk familial adenomatous polyposis (FAP) dan sindrom Lynch (hereditary nonpolyposis colorectal cancer/HNPCC). Di Indonesia, analisis genetik menunjukkan adanya frekuensi tinggi sindrom Lynch yang diduga berperan dalam karakteristik kanker kolorektal pada populasi Indonesia (Susanti et al., dikutip dalam penelitian Yogyakarta, 2024).
Faktor yang dapat dimodifikasi meliputi pola makan tinggi lemak dan daging olahan, rendah serat, obesitas, kurangnya aktivitas fisik, merokok, dan konsumsi alkohol. Penelitian skrining di Semarang menunjukkan bahwa kelainan indeks massa tubuh (body mass index/BMI) berupa kelebihan berat badan dan obesitas meningkatkan risiko kanker kolorektal dan adenoma secara signifikan (OR 10,968; 95% CI 2,33–51,55), demikian pula riwayat keluarga dengan keganasan (OR 18,800; 95% CI 5,13–68,85) (Purnomo et al., 2023). Infeksi Helicobacter pylori juga telah diidentifikasi sebagai faktor risiko potensial untuk rekurensi polip kolorektal (Zhang et al., 2025).
Gejala: Sering Tanpa Keluhan
Sebagian besar polip usus tidak menimbulkan gejala dan ditemukan secara kebetulan saat kolonoskopi skrining atau pemeriksaan untuk indikasi lain. Inilah mengapa skrining rutin menjadi sangat penting. Ketika gejala muncul, biasanya polip sudah berukuran cukup besar atau telah mengalami perubahan ke arah keganasan.
Gejala yang mungkin muncul antara lain perdarahan rektum (darah merah segar atau gelap pada tinja), perubahan pola buang air besar yang berlangsung lebih dari seminggu (diare atau konstipasi), nyeri perut, dan anemia defisiensi besi yang tidak dapat dijelaskan penyebabnya. Perlu diingat bahwa gejala-gejala ini tidak spesifik dan dapat disebabkan oleh banyak kondisi lain, sehingga evaluasi medis diperlukan untuk memastikan diagnosis.
Diagnosis dan Klasifikasi Endoskopik
Kolonoskopi merupakan standar baku emas (gold standard) untuk deteksi dan diagnosis polip usus. Selain memungkinkan visualisasi langsung seluruh kolon dan rektum, kolonoskopi juga memungkinkan pengambilan biopsi dan pengangkatan polip dalam satu prosedur.
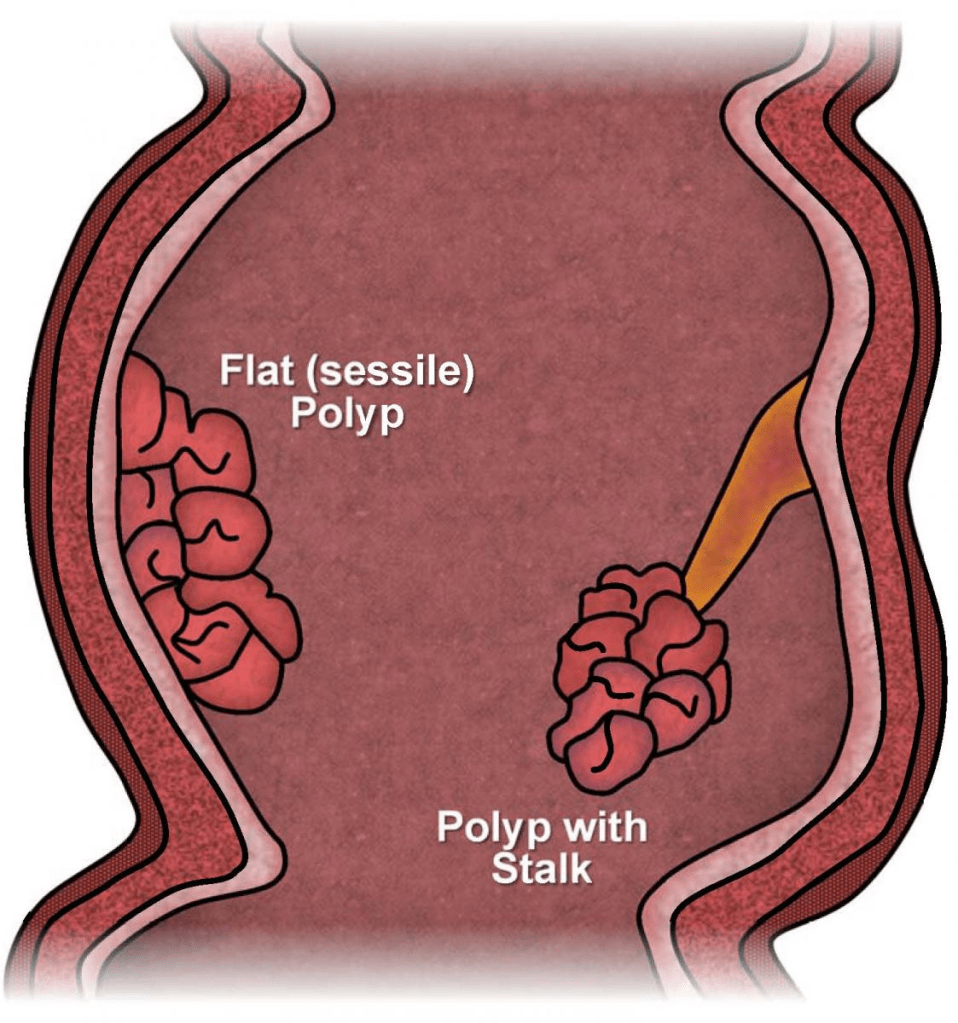
Kemajuan teknologi endoskopik telah memungkinkan diagnosis optik polip secara real-time. Beberapa sistem klasifikasi endoskopik yang digunakan secara luas meliputi klasifikasi Paris yang mendeskripsikan morfologi polip menjadi polipoid (bertangkai/pedunkulata, sesil, sub-pedunkulata) dan non-polipoid (datar-elevasi, datar, depresif), klasifikasi NICE (NBI International Colorectal Endoscopic) yang menggunakan narrow band imaging untuk memprediksi histologi polip, klasifikasi pola pit Kudo yang mengevaluasi pola permukaan menggunakan kromoskopi, serta klasifikasi JNET (Japan NBI Expert Team) yang dikembangkan untuk membedakan antara lesi serasi dan adenoma konvensional (Ferlitsch et al., 2024; Ginsberg et al., 2024).
Panduan terbaru dari European Society of Gastrointestinal Endoscopy (ESGE) tahun 2024 merekomendasikan penggunaan klasifikasi NICE dan JNET sebagai alat bantu diagnosis optik untuk menentukan jenis polip dan memandu keputusan tata laksana selama prosedur endoskopi (Ferlitsch et al., 2024). Perkembangan kecerdasan buatan (artificial intelligence/AI) dalam deteksi polip juga menunjukkan potensi yang menjanjikan untuk meningkatkan ADR dan kualitas kolonoskopi secara keseluruhan (Hann et al., 2024).
Tata Laksana: Angkat Sebelum Menjadi Kanker
Prinsip utama tata laksana polip usus adalah pengangkatan seluruh polip yang ditemukan selama kolonoskopi — sebuah pendekatan yang telah terbukti mampu mengurangi mortalitas akibat kanker kolorektal hingga sekitar 53% (Zauber et al., 2012). Teknik polipektomi yang dipilih bergantung pada ukuran, morfologi, dan karakteristik polip.
Untuk polip kecil (diminutif, ≤5 mm), polipektomi menggunakan cold snare merupakan teknik yang direkomendasikan. Forsep biopsi dingin (cold biopsy forceps) dapat dipertimbangkan sebagai pilihan kedua, tetapi hanya untuk polip berukuran ≤3 mm. Untuk polip berukuran 6–19 mm tanpa tanda invasi submukosa, cold snare polypectomy tetap menjadi pilihan utama. Untuk polip berukuran ≥20 mm, reseksi mukosa endoskopik (endoscopic mucosal resection/EMR) diperlukan. Pada polip pedunkulata (bertangkai), hot snare tetap menjadi standar baku, dengan pertimbangan hemostasis profilaksis untuk polip dengan kepala ≥2 cm atau tangkai ≥1 cm (Ferlitsch et al., 2024; Ginsberg et al., 2024).
Polip yang menunjukkan tanda-tanda invasi submukosa berdasarkan klasifikasi NICE tipe 3 atau pola pit Kudo tipe V memerlukan pertimbangan khusus. Untuk kasus tertentu, diseksi submukosa endoskopik (endoscopic submucosal dissection/ESD) dapat dilakukan oleh endoskopis berpengalaman, terutama untuk lesi rektum yang besar. Namun, kolektomi tetap menjadi standar perawatan untuk lesi yang lebih lanjut atau memiliki faktor risiko metastasis kelenjar getah bening (Dang et al., 2023).
Skrining: Kunci Pencegahan
Skrining kanker kolorektal merupakan strategi yang telah terbukti efektif dalam mengurangi insiden dan mortalitas kanker kolorektal. US Preventive Services Task Force (USPSTF) merekomendasikan skrining dimulai pada usia 45 tahun untuk individu dengan risiko rata-rata, sebuah perubahan dari rekomendasi sebelumnya yang memulai skrining pada usia 50 tahun. Perubahan ini didorong oleh peningkatan insiden kanker kolorektal pada dewasa muda (Davidson et al., 2021).
Metode skrining yang tersedia meliputi tes darah samar tinja imunokimia (immunochemical fecal occult blood test/iFOBT atau FIT) yang direkomendasikan setiap tahun dan merupakan metode skrining yang paling sering diimplementasikan dalam program skrining berbasis populasi, kolonoskopi yang direkomendasikan setiap 10 tahun dan merupakan metode paling komprehensif, sigmoidoskopi fleksibel setiap 5 tahun, serta tes DNA tinja multitarget (multitarget stool DNA test) setiap 3 tahun.
Di Indonesia, program skrining kanker kolorektal berbasis layanan kesehatan primer masih dalam tahap pengembangan. Penelitian di Semarang menunjukkan bahwa prevalensi iFOBT positif di fasilitas kesehatan primer cukup tinggi (16,7%), namun kepatuhan untuk menjalani kolonoskopi lanjutan masih perlu ditingkatkan (Purnomo et al., 2023). Pedoman Nasional Pelayanan Kedokteran Tata Laksana Kanker Kolorektal dari Kementerian Kesehatan RI tahun 2018 menjadi acuan utama penatalaksanaan di tingkat nasional, meskipun pembaruan diperlukan mengingat perkembangan bukti ilmiah terbaru.
Surveilans Pasca-Polipektomi
Setelah pengangkatan polip, surveilans kolonoskopi berkala diperlukan untuk mendeteksi polip baru (metachronous) atau rekurensi. Interval surveilans ditentukan berdasarkan temuan pada kolonoskopi indeks, dengan mempertimbangkan jumlah, ukuran, histologi, dan lokasi polip.
Berdasarkan rekomendasi terbaru dari US Multi-Society Task Force on Colorectal Cancer (USMSTF) tahun 2020, pasien dengan satu hingga dua adenoma kecil (<10 mm) dengan displasia tingkat rendah direkomendasikan menjalani kolonoskopi ulang dalam 7–10 tahun, adenoma lanjut (≥10 mm, komponen vilosa, atau displasia tingkat tinggi) dalam 3 tahun, tiga hingga empat adenoma kecil dalam 3–5 tahun, lima hingga sepuluh adenoma dalam 3 tahun, serta lebih dari sepuluh adenoma dalam 1 tahun dengan pertimbangan evaluasi genetik (Gupta et al., 2020).
Untuk polip serasi, lesi serasi sesil berukuran ≥10 mm atau dengan displasia memerlukan surveilans dalam 3 tahun, sedangkan lesi serasi sesil kecil tanpa displasia dapat menjalani surveilans dalam 5 tahun. Panduan serupa juga diterbitkan oleh ESGE, BSG/ACPGBI, dan JGES, dengan perbedaan kecil pada interval tertentu (Yoon et al., 2023).
Pasca-reseksi parsial (piecemeal) untuk polip berukuran lebih dari 20 mm, pemeriksaan ulang lokasi direkomendasikan dalam 3–6 bulan untuk memastikan reseksi lengkap, mengingat risiko rekurensi lokal yang lebih tinggi.
Pencegahan: Gaya Hidup Sehat sebagai Investasi
Meskipun beberapa faktor risiko polip usus tidak dapat dimodifikasi, banyak langkah yang dapat diambil untuk mengurangi risiko. Panduan National Comprehensive Cancer Network (NCCN) tahun 2024 merekomendasikan beberapa strategi pencegahan: mengonsumsi makanan kaya nabati dan berserat tinggi, membatasi konsumsi daging merah dan makanan olahan, membatasi atau menghindari konsumsi alkohol, menjaga berat badan ideal, meningkatkan aktivitas fisik secara teratur, serta berhenti merokok.
Beberapa penelitian juga menunjukkan efek protektif dari konsumsi kalsium, vitamin D, dan produk susu terhadap risiko kanker kolorektal, meskipun bukti ini masih terus berkembang.
Penutup
Polip usus adalah kondisi yang sangat umum ditemukan, namun penanganannya tidak boleh dianggap remeh. Sebagian kecil polip — terutama adenoma lanjut dan lesi serasi sesil — memiliki potensi nyata untuk bertransformasi menjadi kanker kolorektal jika dibiarkan tanpa pengobatan. Di Indonesia, di mana program skrining kanker kolorektal masih belum merata dan kesadaran masyarakat masih perlu ditingkatkan, edukasi tentang pentingnya deteksi dini menjadi sangat krusial.
Pesan utama yang perlu diingat adalah bahwa sebagian besar kanker kolorektal dapat dicegah melalui deteksi dan pengangkatan polip sebelum polip tersebut berkembang menjadi kanker. Skrining yang tepat waktu, gaya hidup sehat, dan kepatuhan terhadap jadwal surveilans pasca-polipektomi merupakan tiga pilar utama dalam strategi pencegahan kanker kolorektal.
Referensi
Correa, P. (2005). Epidemiology of colorectal polyps. PubMed. https://pubmed.ncbi.nlm.nih.gov/15666099/
Crockett, S. D., & Nagtegaal, I. D. (2019). Terminology, molecular features, epidemiology, and management of serrated colorectal neoplasia. Gastroenterology, 157(4), 949–966.e4. https://doi.org/10.1053/j.gastro.2019.09.036
Dang, H., Bhattacharyya, R., & Bhatt, A. (2023). Colorectal polyp classification and management of complex polyps for surgeon endoscopists. Canadian Journal of Surgery, 66(5), E428–E436. https://doi.org/10.1503/cjs.014622
Davidson, K. W., Barry, M. J., Mangione, C. M., et al. (2021). Screening for colorectal cancer: US Preventive Services Task Force recommendation statement. JAMA, 325(19), 1965–1977. https://doi.org/10.1001/jama.2021.6238
Ferlitsch, M., et al. (2024). Colorectal polypectomy and endoscopic mucosal resection (EMR): ESGE Guideline. Endoscopy. European Society of Gastrointestinal Endoscopy. https://www.esge.com/assets/downloads/pdfs/guidelines/2024_a-2304-3219.pdf
Ginsberg, G. G., et al. (2024). AGA Clinical Practice Update on appropriate and tailored polypectomy: Expert review. Clinical Gastroenterology and Hepatology, 22(3), 470–489. https://doi.org/10.1016/j.cgh.2023.10.012
Gupta, S., Lieberman, D., Anderson, J. C., et al. (2020). Recommendations for follow-up after colonoscopy and polypectomy: A consensus update by the US Multi-Society Task Force on Colorectal Cancer. Gastroenterology, 158(4), 1131–1153.e5. https://doi.org/10.1053/j.gastro.2019.10.026
Hann, A., et al. (2024). Colon polyps: Updates in classification and management. Current Opinion in Gastroenterology, 40(1), 14–20. https://doi.org/10.1097/MOG.0000000000000988
Kementerian Kesehatan RI. (2018). Pedoman nasional pelayanan kedokteran tata laksana kanker kolorektal. Jakarta: Kementerian Kesehatan RI.
Makmun, D., Simadibrata, M., Abdullah, M., et al. (2021). Colorectal cancer patients in a tertiary hospital in Indonesia: Prevalence of the younger population and associated factors. World Journal of Clinical Cases, 9(33), 9804–9814. https://doi.org/10.12998/wjcc.v9.i33.9804
Murakami, T., Kurosawa, T., Fukushima, H., et al. (2022). Sessile serrated lesions: Clinicopathological characteristics, endoscopic diagnosis, and management. Digestive Endoscopy, 34(6), 1096–1109. https://doi.org/10.1111/den.14283
Purnomo, H. D., Permatadewi, C. O., Prasetyo, A., et al. (2023). Colorectal cancer screening in Semarang, Indonesia: A multicenter primary health care based study. PLoS ONE, 18(1), e0279570. https://doi.org/10.1371/journal.pone.0279570
Sinaga, E. S., Rahayu, S., Susanti, S., et al. (2021). Genetic risk factors for colorectal cancer in multiethnic Indonesians. Scientific Reports, 11, 9988. https://doi.org/10.1038/s41598-021-88805-4
Sullivan, B. A., Noujaim, M., & Roper, J. (2022). Cause, epidemiology, and histology of polyps and pathways to colorectal cancer. Gastrointestinal Endoscopy Clinics of North America, 32(2), 177–194. https://doi.org/10.1016/j.giec.2021.12.001
Yoon, J. Y., et al. (2023). Summary and comparison of recently updated post-polypectomy surveillance guidelines. Korean Journal of Internal Medicine, 38(6), 789–799. https://doi.org/10.3904/kjim.2023.310
Zauber, A. G., Winawer, S. J., O’Brien, M. J., et al. (2012). Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. New England Journal of Medicine, 366(8), 687–696. https://doi.org/10.1056/NEJMoa1100370
Zhang, Y., et al. (2025). Study on the risk factors for colorectal polyp recurrence. Frontiers in Medicine, 12, 1553194. https://doi.org/10.3389/fmed.2025.1553194

Tinggalkan komentar