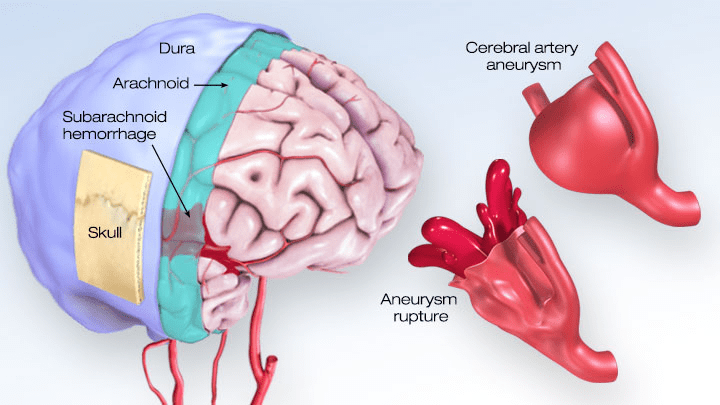
Perdarahan subaraknoid (subarachnoid haemorrhage/SAH) adalah salah satu kondisi kegawatdaruratan neurologis paling serius yang dapat menimpa siapa saja, umumnya di usia produktif. Meski hanya mencakup sekitar 5–10% dari seluruh kejadian stroke, dampaknya sangat besar karena angka kematiannya tinggi dan banyak penyintas yang mengalami kecacatan jangka panjang. Kondisi ini terjadi ketika darah merembes ke ruang subaraknoid — ruang sempit berisi cairan serebrospinal yang menyelimuti permukaan otak — biasanya akibat pecahnya aneurisma pada pembuluh darah otak.
Seberapa Sering SAH Terjadi?
Secara global, insidensi SAH diperkirakan sekitar 6,1 per 100.000 orang per tahun, dengan prevalensi global mencapai 8,09 juta kasus berdasarkan data Global Burden of Disease (GBD) 2021. Menariknya, angka ini sangat bervariasi antarwilayah. Jepang dan Finlandia memiliki insidensi tertinggi di dunia, masing-masing sebesar 28 dan 16,6 per 100.000 orang per tahun (Hoh dkk., 2023). Di sisi lain, tren global menunjukkan penurunan angka insidensi terstandarisasi usia (age-standardized incidence rate/ASIR) dengan perubahan persentase tahunan (EAPC) sebesar -1,52 antara tahun 1990 hingga 2021. Angka kematian dan disability-adjusted life years (DALYs) juga menurun dalam periode yang sama (Lv dkk., 2024).
Meskipun tren global cenderung membaik, beban penyakit yang nyata justru meningkat di negara-negara berpendapatan rendah dan menengah, termasuk kawasan Asia Tenggara. Faktor risiko utama — yakni hipertensi dan merokok — masih sangat lazim di wilayah ini, sehingga upaya pencegahan tetap menjadi prioritas.
SAH biasanya muncul pada usia rata-rata sekitar 55 tahun, dengan kecenderungan lebih tinggi pada perempuan, terutama pada kelompok usia di atas 50 tahun. Angka mortalitas keseluruhan tetap tinggi, mencapai 25–35%, dan sekitar seperempat pasien meninggal sebelum sempat tiba di rumah sakit (Claassen & Park, 2022).
Apa Penyebab SAH?
Penyebab tersering SAH spontan adalah pecahnya aneurisma intrakranial, yang bertanggung jawab atas sekitar 80–85% kasus. Aneurisma adalah penonjolan abnormal pada dinding pembuluh darah arteri di otak yang terbentuk akibat kelemahan struktural dinding pembuluh darah. Diperkirakan sekitar 1–2% populasi umum memiliki aneurisma intrakranial, namun sebagian besar tidak bergejala sampai terjadi ruptur (Thilak dkk., 2024).
Sekitar 10% SAH spontan termasuk jenis perimesensefalik (perimesencephalic), di mana perdarahan terbatas di sekitar batang otak bagian depan dan memiliki prognosis yang jauh lebih baik. Sisanya sekitar 5% disebabkan oleh berbagai kondisi langka seperti malformasi arteriovenosa, vaskulitis, dan diseksi arteri (Claassen & Park, 2022).
Faktor risiko yang paling kuat terkait dengan SAH meliputi hipertensi, merokok, dan konsumsi alkohol berlebihan. Tekanan darah sistolik tinggi merupakan faktor risiko kunci, dan diperkirakan hingga 72% beban penyakit SAH dapat dicegah dengan mengeliminasi faktor risiko utamanya — terutama hipertensi dan merokok (Lv dkk., 2024). Penggunaan kokain, riwayat keluarga dengan aneurisma serebral (terutama jika dua atau lebih kerabat dekat terpengaruh), serta ukuran aneurisma lebih dari 7 mm juga meningkatkan risiko. Adanya daughter sac (tonjolan tidak beraturan pada dinding aneurisma) dan rasio ukuran aneurisma terhadap pembuluh darah yang besar turut meningkatkan risiko ruptur (Thilak dkk., 2024).
Bagaimana SAH Bermanifestasi Secara Klinis?
Gejala klasik SAH yang paling khas adalah nyeri kepala mendadak yang sangat hebat — sering digambarkan oleh pasien sebagai “nyeri kepala terburuk dalam hidup saya” (thunderclap headache). Nyeri ini mencapai intensitas maksimal dalam hitungan detik hingga menit dan berbeda secara fundamental dari nyeri kepala biasa yang memiliki onset bertahap.
Selain nyeri kepala, gejala lain yang sering menyertai meliputi kaku kuduk (meningismus) akibat iritasi darah pada selaput otak, mual dan muntah, penurunan kesadaran yang dapat bersifat sementara maupun berkepanjangan, defisit neurologis fokal seperti kelemahan anggota gerak atau kelumpuhan saraf kranial, dan kejang. Hingga 43% kasus SAH didahului oleh nyeri kepala peringatan (sentinel headache) dalam beberapa hari hingga minggu sebelum ruptur utama, yang sering kali tidak terdeteksi atau dianggap remeh oleh pasien maupun dokter (Hoh dkk., 2023).
Untuk menyingkirkan diagnosis SAH pada pasien yang datang dengan nyeri kepala onset mendadak, Ottawa SAH Rule menjadi alat klinis yang berguna. Pada pasien usia 15 tahun ke atas yang sadar penuh dengan nyeri kepala mendadak nontraumatik yang mencapai intensitas maksimal dalam 1 jam, SAH dapat disingkirkan jika tidak ditemukan satu pun dari kriteria berikut: usia 40 tahun atau lebih, nyeri atau kekakuan leher, kehilangan kesadaran yang disaksikan, onset saat aktivitas fisik, nyeri kepala tipe thunderclap, atau keterbatasan fleksi leher pada pemeriksaan fisik.
Bagaimana SAH Didiagnosis?
Pendekatan diagnostik untuk SAH dimulai dengan computed tomography (CT) kepala tanpa kontras. Pada era pencitraan modern, sensitivitas CT kepala dalam mendeteksi SAH sangat tinggi jika dilakukan dalam 6 jam pertama setelah onset gejala. Pedoman AHA/ASA 2023 menyatakan bahwa CT kepala tanpa kontras yang dilakukan dalam 6 jam pada pasien tanpa defisit neurologis cukup untuk menyingkirkan SAH (Hoh dkk., 2023).
Namun, jika CT kepala dilakukan setelah 6 jam atau jika hasil CT negatif namun kecurigaan klinis tetap tinggi, langkah selanjutnya yang direkomendasikan adalah pungsi lumbal untuk mendeteksi adanya xantokromia (perubahan warna kekuningan pada cairan serebrospinal akibat degradasi hemoglobin). AHA/ASA secara tegas merekomendasikan pungsi lumbal sebagai langkah diagnostik lanjutan setelah CT negatif, meskipun beberapa pusat kesehatan juga mempertimbangkan CT angiografi (CTA) sebagai alternatif. Perlu dicatat bahwa CTA memiliki sensitivitas yang tidak sempurna dalam mendeteksi aneurisma kecil, sehingga hasil negatif tidak sepenuhnya menyingkirkan SAH (Hoh dkk., 2023).
CT angiografi dan digital subtraction angiography (DSA) selanjutnya digunakan untuk mengidentifikasi dan melokalisasi sumber perdarahan, khususnya aneurisma yang pecah. DSA tetap menjadi standar baku emas (gold standard) untuk mendeteksi aneurisma intrakranial, meskipun CTA modern memberikan kualitas pencitraan yang sangat baik dan bersifat kurang invasif (Thilak dkk., 2024).
Bagaimana Tingkat Keparahan SAH Dinilai?
Penilaian derajat keparahan SAH sangat penting untuk menentukan prognosis dan memandu pengambilan keputusan klinis. Beberapa sistem penilaian yang umum digunakan meliputi skala Hunt and Hess yang mengklasifikasikan keparahan berdasarkan gejala klinis dari derajat I (nyeri kepala ringan) hingga derajat V (koma dalam), skala World Federation of Neurosurgical Societies (WFNS) yang berbasis pada Glasgow Coma Scale (GCS), dan skala modified Fisher yang menilai beban perdarahan berdasarkan gambaran CT (Thilak dkk., 2024).
Skala WFNS menjadi skala yang paling direkomendasikan untuk penilaian klinis. Skor berat (derajat 4 dan 5) pada skala ini menunjukkan luaran yang buruk. Sementara itu, skala modified Fisher membantu memprediksi risiko vasospasme serebral yang merupakan komplikasi serius pascaperdarahan. Sistem penilaian yang lebih baru seperti SEBES, Hidjra, dan VASOGRADE juga mulai diadopsi untuk melengkapi evaluasi prognostik (Thilak dkk., 2024).
Bagaimana SAH Ditangani?
Tata laksana SAH memerlukan pendekatan multidisipliner yang mencakup beberapa fase kritis.
Stabilisasi awal dan pencegahan perdarahan ulang. Dalam 24 jam pertama, prioritas utama adalah diagnosis cepat, stabilisasi kondisi pasien, dan penanganan definitif aneurisma yang pecah. Perdarahan ulang (rebleeding) merupakan komplikasi paling mematikan, dengan risiko tertinggi dalam 24 jam pertama. Pengamanan aneurisma secara dini — baik melalui pembedahan maupun prosedur endovaskular — sangat penting karena perdarahan ulang membawa risiko mortalitas yang sangat tinggi (Robba dkk., 2024).
Dua modalitas utama untuk mengamankan aneurisma adalah surgical clipping (pembedahan terbuka untuk menjepit leher aneurisma) dan endovascular coiling (memasukkan koil platinum melalui kateter untuk mengisi dan menutup aneurisma dari dalam). Uji klinis International Subarachnoid Aneurysm Trial (ISAT) menunjukkan bahwa coiling endovaskular dikaitkan dengan luaran yang lebih baik dibandingkan clipping pada pasien tertentu, dan saat ini prosedur endovaskular menjadi pilihan yang semakin dominan. Namun, keputusan antara kedua modalitas ini harus mempertimbangkan karakteristik pasien dan aneurisma secara individual (Hoh dkk., 2023).
Pedoman AHA/ASA 2023 menekankan bahwa penanganan sebaiknya dilakukan di pusat stroke yang menangani lebih dari 35 kasus SAH per tahun, karena volume kasus yang tinggi dikaitkan dengan luaran yang lebih baik (Hoh dkk., 2023).
Perawatan intensif dan pencegahan komplikasi. Setelah aneurisma diamankan, perawatan intensif berfokus pada pencegahan dan penanganan komplikasi. Manajemen tekanan darah menjadi krusial — hipertensi harus dikontrol dengan agen kerja pendek untuk mencegah perdarahan ulang sebelum aneurisma diamankan, sementara hipotensi harus dihindari untuk menjaga perfusi serebral. Euvolemia (keseimbangan cairan tubuh) harus dipertahankan untuk mengoptimalkan aliran darah ke otak (Hoh dkk., 2023; Robba dkk., 2024).
Nimodipin, sebuah antagonis kalsium, diberikan secara oral selama 21 hari sebagai satu-satunya agen farmakologis yang terbukti memperbaiki luaran fungsional pada SAH, meskipun mekanisme pastinya mungkin tidak melalui pencegahan vasospasme secara langsung melainkan melalui efek neuroprotektif. Standar kualitas nasional merekomendasikan pemberian nimodipin dalam 24 jam pertama setelah masuk rumah sakit (Thilak dkk., 2024).
Vasospasme serebral dan iskemia serebral tertunda. Vasospasme serebral — penyempitan pembuluh darah arteri otak — merupakan komplikasi serius yang biasanya terjadi antara hari ke-4 hingga ke-14 pascaperdarahan. Jika tidak ditangani, vasospasme dapat berkembang menjadi iskemia serebral tertunda (delayed cerebral ischaemia/DCI), yang merupakan penyebab utama kecacatan dan kematian pada pasien yang berhasil melewati fase awal (Robba dkk., 2024).
Pemantauan vasospasme dilakukan melalui transcranial Doppler (TCD) yang merupakan prosedur noninvasif di sisi tempat tidur, CTA, CT perfusi, atau elektroensefalografi kontinu. Setelah vasospasme terdeteksi, strategi penanganan meliputi pemeliharaan euvolemia, augmentasi tekanan darah, serta terapi invasif seperti pemberian vasodilator intraarterial dan angioplasti serebral pada kasus yang refrakter (Hoh dkk., 2023; Thilak dkk., 2024).
Komplikasi lain. Hidrosefalus terjadi pada sejumlah besar pasien SAH akibat gangguan sirkulasi cairan serebrospinal oleh bekuan darah, dan sering memerlukan pemasangan drainase ventrikel eksternal (external ventricular drain/EVD). Kejang dapat terjadi pada fase akut, meskipun penggunaan profilaksis obat antikejang secara rutin tidak direkomendasikan oleh pedoman terbaru. Gangguan elektrolit — khususnya hiponatremia — serta komplikasi kardiopulmoner juga memerlukan perhatian khusus dalam perawatan intensif (Thilak dkk., 2024; Robba dkk., 2024).
Bagaimana Prognosis dan Pemulihan SAH?
Prognosis SAH bervariasi sangat luas, dari pemulihan penuh hingga kecacatan berat atau kematian. Faktor-faktor yang memengaruhi luaran meliputi usia pasien, tingkat keparahan pada saat masuk (skala WFNS/Hunt and Hess), volume perdarahan, terjadinya komplikasi seperti DCI, perdarahan ulang, dan hidrosefalus, serta kondisi kesehatan penyerta seperti hiperglikemia, sepsis, dan demam (Thilak dkk., 2024).
Aspek yang sering kurang mendapat perhatian adalah luaran neuropsikiatri jangka panjang. Bahkan pada pasien yang mengalami pemulihan fungsional yang baik (skor modified Rankin Scale ≤ 2), gangguan kognitif tetap sangat umum ditemukan. Sebuah studi terbaru menunjukkan bahwa 30% pasien dengan pemulihan fungsional yang baik masih mengalami luaran kognitif yang buruk (Sagues dkk., 2025). Gangguan kognitif, depresi, kecemasan, dan penurunan kualitas hidup merupakan sekuele jangka panjang yang signifikan dan berkontribusi pada hilangnya produktivitas selama bertahun-tahun, mengingat SAH menyerang pada usia produktif (Claassen & Park, 2022).
Pedoman AHA/ASA 2023 secara khusus menambahkan bagian tentang pemulihan sebagai penekanan baru, merekomendasikan skrining untuk gangguan psikologis, seksual, dan kognitif pascarawatan guna meningkatkan kualitas hidup pasien (Hoh dkk., 2023).
Konteks Indonesia dan Tantangan ke Depan
Di Indonesia, tantangan dalam penanganan SAH meliputi keterbatasan akses terhadap pusat neurovaskular bervolume tinggi di banyak daerah, keterlambatan rujukan dan diagnosis akibat keterbatasan fasilitas pencitraan di rumah sakit perifer, serta masih tingginya prevalensi faktor risiko utama yaitu hipertensi dan merokok dalam populasi.
Data dari studi beban penyakit global menunjukkan bahwa negara-negara berpendapatan rendah dan menengah di Asia Tenggara mengalami peningkatan jumlah absolut kasus SAH seiring dengan pertumbuhan dan penuaan populasi (Lv dkk., 2024). Upaya pencegahan melalui pengendalian hipertensi dan penghentian merokok tetap menjadi strategi paling efektif dan cost-effective untuk mengurangi beban SAH di Indonesia.
Perkembangan telemedisin dan teknologi baru yang ditawarkan dalam pedoman terkini memberikan harapan untuk mengatasi kesenjangan kesehatan dalam penanganan SAH, khususnya di wilayah dengan akses terbatas terhadap spesialis neurovaskular (Thilak dkk., 2024). Peningkatan kesadaran masyarakat tentang pentingnya mengenali gejala nyeri kepala mendadak yang sangat hebat sebagai tanda kegawatdaruratan, serta penguatan sistem rujukan yang efisien, menjadi langkah-langkah strategis yang perlu terus didorong dalam konteks sistem kesehatan Indonesia.
Daftar Referensi
Claassen, J., & Park, S. (2022). Spontaneous subarachnoid haemorrhage. The Lancet, 400(10355), 846–862. https://doi.org/10.1016/S0140-6736(22)00938-2
Hoh, B. L., Ko, N. U., Amin-Hanjani, S., Chou, S. H.-Y., Cruz-Flores, S., Dangayach, N. S., Derdeyn, C. P., Du, R., Hänggi, D., Hetts, S. W., Ifejika, N. L., Johnson, R., Keigher, K. M., Leslie-Mazwi, T. M., Lucke-Wold, B., Rabinstein, A. A., Robicsek, S. A., Stapleton, C. J., Suarez, J. I., … Welch, B. G. (2023). 2023 Guideline for the management of patients with aneurysmal subarachnoid hemorrhage: A guideline from the American Heart Association/American Stroke Association. Stroke, 54(7), e314–e370. https://doi.org/10.1161/STR.0000000000000436
Lv, B., Lan, J. X., Si, Y. F., Lan, G. C., Wang, B. J., Li, Z. H., Ma, C., & Li, Y. S. (2024). Epidemiological trends of subarachnoid hemorrhage at global, regional, and national level: A trend analysis study from 1990 to 2021. Military Medical Research, 11, 46. https://doi.org/10.1186/s40779-024-00551-6
Robba, C., Busl, K. M., Claassen, J., Diringer, M. N., Helbok, R., Park, S., Rabinstein, A., Treggiari, M., Vergouwen, M. D. I., & Citerio, G. (2024). Contemporary management of aneurysmal subarachnoid haemorrhage: An update for the intensivist. Intensive Care Medicine, 50(5), 646–664. https://doi.org/10.1007/s00134-024-07387-7
Sagues, E., Shenoy, N., Van Dam, A., Diaz, L., Gudino, A., Dier, C., Cifuentes, D., Calle, R., Wendt, L., Dlouhy, K., Zanaty, M., Ortega-Gutierrez, S., Garcia-Casares, N., & Samaniego, E. A. (2025). Volume of aneurysmal subarachnoid hemorrhage and cognitive outcomes. Neurocritical Care, 44(1), 203–211. https://doi.org/10.1007/s12028-025-02326-w
Thilak, S., Brown, P., Whitehouse, T., Gautam, N., Lawrence, E., Ahmed, Z., & Veenith, T. (2024). Diagnosis and management of subarachnoid haemorrhage. Nature Communications, 15(1), 1850. https://doi.org/10.1038/s41467-024-46015-2

Tinggalkan komentar